|
|
|
|
|
 |
|
유전자재조합식품의안전성평가심사의뢰서
|
|
|
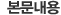 |
[별지 제1호서식]
유전자재조합 식품의 안전성평가 심사 의뢰서
처리기간
270일
신청자
①회사명
② 사업자등록번호
③주소
④ 대표자명
⑤ 전화연락처
개발자
⑥ 개발사명
⑦주소
⑧구분
제3조 제________호
제품종류
(Organism)
품목명
(Event/line명)
상품명
(Brand 명)
⑫ 부여된 특성
⑬ 삽입된 유전자
⑭ 최초 시장유통 승인국가 및 승인연도
⑮그 밖의 시장유통 승인 국가 및 승인연도
안전성 심사 중인 국가 및 신청일시
생산 현황 구분
신규 ()․ 상업적 생산 중단 ()
용도(식용)
수입 ()․ 개발( )․생산 ()․ 기타 ()
식품위생법 제15조의 규정에 의하여 유전자재조합 식품의 안전성 평가를 심사 의뢰합니다.
년월일
신청자 인
식품의약품안전청장 귀하
구비서류등
1. 요약보고서 각 2부 (외국어자료는 원문과 번역문)
2. 유전자재조합체의 개발목적 및 이용방법에 관한 자료
3. 숙주에 관한 자료
4. 공여체에 관한 자료
5. 유전자재조합체에 관한 자료
6. 유전자재조합체의 특성에 관한 자료
7. 기타 안전성 평가에 관한 자료
8. 분석방법에 대한 관련 자료 및 표준품
수수료
300만원
기재상 주의사항
1. ① 내지 ⑦항에 변경사항이 발생할 경우 신고 사항으로 인정
(뒷면)
2. ⑧항의 구분은 지침 제3조에 따라 해당하는 다음 각 호의 번호를 기입한다.
.... |
|
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
| |
|
|
|
