|
|
|
|
|
 |
|
무기소재 - 코발트[Co(NH3)4CO3]NO3 착물 합성 실험
|
|
|
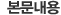 |
[Co(NH3)4CO3]NO3
목 차
-실 험 목 적
-실 험 이 론
-실 험 방 법
-실 험 결 과
-고 찰
실 험 목 적
[Co(OH2)6(NO3)2 로부터 착물의 합성을 통해 [Co(NH3)4(CO)3]NO3 생성물을 얻어 그 구조와 특성을 파악해보자.
실 험 이 론
ⅰ) 적외선 분광계 (FT-IR)ⅱ) 자외선- 가시광선 분광계 (UV-VIS)ⅲ) 전도도 측정
Co(II)착물은 리간드의 교환이 빠르게 이루어지는 반응이며 첫 단계는 Co(OH2)62+ + 4NH3 + CO32- Co(NH3)4CO3 + 6H2O 이다. 여기서 Co(II)착물은 Co(II)이온 즉 [Co(NH3)4CO3]+에서 주어진 H2O2의 전자를 받아서 산화된다
[Co(NH3)4CO3]NO3
Cobalt compound
① Cobalt의 전자 배치 : [Ar] 3d74s2
② Cobalt 산화 상태 : Ⅰ, Ⅱ, Ⅲ, Ⅳ
Cobalt(코발트)
1) Co(Ⅰ) : p-결합 리간드와 착물 형성,
제일 계열의 전이원소에서 보기 드문 특징
2) Co(Ⅱ) : 팔면체와 사면체를 모두 형성하나,
모두 치환성이 있으며, 산소분자에 의하여
산화되는 경향이 크다.
이들의 착물은 공기의 접촉을 피하며 제조하여야 한다
2) Co(Ⅲ) : 착화제가 없는 수용액에서는 Co(Ⅲ)는 Co(Ⅱ)로 환원
암모니아 같은 착화제가 존재할 때 더 안정함
Infrared Spectroscopy
적외선 영역이란
적외선 영역의 파장은 0.75m ~25m 이며
분석에 쓰이는 적외선 파장은 2.5m~15m에 해당한다
적외선 분광학(Infrared Spectroscopy)
.... |
|
|
|
 |
|
|
|
|
|
|
|
|
|
|
|
| |
|
|
|
